APRENDIENDO DE UN BLOG
TEMA: física y química.......
sábado, 13 de diciembre de 2014
lunes, 22 de septiembre de 2014
¿QUÈ ES UNA COMETA Y cuáles son los más famosos?
Los cometas son «bolas de nieve sucia», que habitan en los confines del Sistema Solar, en una gigantesca envoltura compuesta por la Nube de Oort y el Cinturón de Kuiper, que probablemente se formó, junto al resto de nuestro Sistema Solar, hace unos 4.500 millones de años. Sometidos a la fuerza de la gravedad, como cualquier objeto del Universo, de vez en cuando sucede que choques entre ellos o el «tirón gravitatorio» de una estrella cercana son capaces de arrancarlos de su nube precipitándolos hacia el Sol. Una vez iniciado el viaje, nuevos encuentros gravitatorios definirán su órbita. Una órbita parabólica o hiperbólica (ambas curvas abiertas) significa que el cometa caerá hacia el Sol, lo rodeará y se alejará de él para no volver nunca más. Una órbita elíptica (curva cerrada) nos indica que el cometa volverá y, cuanto menos alargada sea la elipse, menos tiempo tardará en hacerlo.
Pero, también puede ocurrir, que el cometa no sobreviva a su encuentro con el Sol, como ha sido el caso del cometa ISON.
LOS MÁS FAMOSOS
Gran Cometa de 1744: Chéseaux y varios otros observadores reportaron un fenómeno sumamente insólito 'un abanico' de seis colas separadas que sobrepasó el horizonte.
Cometa 3D/Biela: a finales del siglo XIX se partió en dos, y más tarde en fragmentos minúsculos, dando lugar a una lluvia de estrellas, con lo que desapareció para siempre.
Cometa Coggia: obtuvo mucha fama debido a su extraordinaria belleza.
Cometa 67P/Churyumov-Gerasimenko. Destino de la sonda espacial europea Rosetta.
Cometa 2P/Encke
Cometa 1P/Halley: describe su órbita cada 76 años. En 1910 su aproximación a la Tierra, conllevó que su cola rozara con las capas superiores de la atmósfera.
Cometa Luxell: al pasar cerca de Júpiter, perdió parte de su masa y padeció perturbaciones
importantes en su órbita.
Cometa Shoemaker-Levy 9: en 1993 se fragmentó debido al intenso campo gravitorio de Júpiter y acabó impactando contra él.
Cometa 9P/Tempel 1: la sonda espacial Deep Impact lanzó un proyectil sobre este cometa para estudiar la composición de su núcleo.
Cometa 55P/Tempel-Tuttle: progenitor de la lluvia de meteoros de las Leónidas.
Cometa 109P/Swift-Tuttle el progenitor de la lluvia de meteoros de las Perseidas.
Cometa McNaught: visible a simple vista a pleno día.
martes, 3 de junio de 2014
GASES NOBLES
Los gases nobles son un grupo de elementos químicos con propiedades muy similares: bajo condiciones normales, son gases monoatómicos inodoros, incoloros y presentan una reactividad química muy baja. Se sitúan en el grupo 18 (8A) de la tabla periódica (anteriormente llamado grupo 0). Los siete gases nobles que se encuentran en la naturaleza son helio (He), neón (Ne), argón (Ar), kriptón (Kr), xenón (Xe), el radiactivoradón (Rn) y ununoctio (Uuo).
EL MEDIO AMBIENTE
(UNA VERDAD INCÓMODA)
El medio ambiente, es uno de los temas más serios de nuestro planeta.
Creo que todos sabemos que este problema es muy grave pero... a caso ¿hacemos algo?...
sí, muchos países han tomado muchas medidas como Roma, Amsterdam,...
pero hay algunos que no las toman o las toman pero nadie las cumple esto es un error del se humano. Uno de los países más contaminates es Estados Unidos tanto como China o brasil que destaca por la deforestación de sus selvas. No podemos esperar más hay que tomar más medidas y no sólo tomarlas sino también cumplirlas, y disminuir la gran emisión de CO2.
China es un país que emite mucho CO2 por sus centrales nucleares, sus numerosas industrias que emiten mucha cantidad de CO2, también la deforestación de selvas y bosques disminuye la emisión de oxígeno.
aqui tenemos una foto de las consecuencias:
ESTA ES UNA DEFORESTACIÓN
ESTA ES UNA DEFORESTACIÓN

viernes, 18 de abril de 2014
MERCURIO
El mercurio o azogue o ☿ es un elemento químico de número atómico 80. Su nombre y símbolo (Hg) procede de hidrargirio, término hoy ya en desuso, que a su vez procede del latín hydrargyrum y dehydrargyrus, que a su vez proviene del griego hydrargyros (hydros = agua y argyros = plata). El nombre de Mercurio se le dio en honor al dios romano del mismo nombre, que era el mensajero de los dioses, y debido a la movilidad del mercurio se le comparó con este dios.
sábado, 5 de abril de 2014
RUBIDIO
El rubidio es un metal alcalino blando, de color plateado blanco brillante que empaña rápidamente al aire, muy reactivo —es el segundo elemento alcalino más electropositivo y puede encontrarse líquido a temperatura ambiente. Al igual que los demás elementos del grupo 1 puede arder espontáneamente en aire con llama de color violeta amarillento, reacciona violentamente con el agua desprendiendo hidrógeno y forma amalgama con mercurio. Puede formar aleaciones con oro,los demás metales alcalinos, y alcalinotérreos, antimonio y bismuto.
viernes, 4 de abril de 2014
Diez curiosidades químicas cotidianas que deberías conocer.
¿Por qué es roja la carne? ¿Qué hace que la mantequilla rancia huela tan mal? ¿La nuez moscada puede causar alucinaciones? Diez datos químicos que pueden resultarte útiles en tu vida cotidiana.
1. El etileno es un gas producido por la fruta al madurar. Las naranjas son muy sensibles al etileno y se deterioran pronto.
2. El ácido butírico es responsable del desagradable olor de la mantequilla rancia.
3. El lápiz de labios se elabora con cera de abeja y aceite. El aceite suele ser de ricino.
4. La fructosa (azúcar de las frutas) es más dulce que la sacarosa (azúcar de caña).
5. Los jugos gástricos del estómago tienen un pH de 1,6 a 1,8. Son más ácidos que el zumo de limón (2,1).
6. El timol se emplea en la conservación de libros para combatir los hongos. Presente en la naturaleza en el tomillo y el orégano, dos hierbas aromáticas muy usadas para cocinar.
7. La mioglobina es el pigmento responsable del color de la carne roja. La carne de un animal más viejo será más oscura.
8. La miristicina es un alcaloide tóxico presente en la nuez moscada que puede causar alucinaciones.
9. El geraniol es un alcohol natural fragante presente en flores como geranios y rosas. Las abejas lo usan para marcar las flores con néctar.
10. El tungsteno se usa como filamento en las bombillas. Su nombre deriva del sueco tung sten, que significa "piedra pesada". En cuanto a los tubos de neón, el nombre de este elemento empezó a usarse en Nueva York y significa "nuevo".
1. El etileno es un gas producido por la fruta al madurar. Las naranjas son muy sensibles al etileno y se deterioran pronto.
2. El ácido butírico es responsable del desagradable olor de la mantequilla rancia.
3. El lápiz de labios se elabora con cera de abeja y aceite. El aceite suele ser de ricino.
4. La fructosa (azúcar de las frutas) es más dulce que la sacarosa (azúcar de caña).
5. Los jugos gástricos del estómago tienen un pH de 1,6 a 1,8. Son más ácidos que el zumo de limón (2,1).
6. El timol se emplea en la conservación de libros para combatir los hongos. Presente en la naturaleza en el tomillo y el orégano, dos hierbas aromáticas muy usadas para cocinar.
7. La mioglobina es el pigmento responsable del color de la carne roja. La carne de un animal más viejo será más oscura.
8. La miristicina es un alcaloide tóxico presente en la nuez moscada que puede causar alucinaciones.
9. El geraniol es un alcohol natural fragante presente en flores como geranios y rosas. Las abejas lo usan para marcar las flores con néctar.
10. El tungsteno se usa como filamento en las bombillas. Su nombre deriva del sueco tung sten, que significa "piedra pesada". En cuanto a los tubos de neón, el nombre de este elemento empezó a usarse en Nueva York y significa "nuevo".
miércoles, 2 de abril de 2014
Enlaces Químicos
o distintos. Cuando los átomos se unen se dice que forman enlaces. La fuerza con la que se unen los átomos depende del tipo o naturaleza de los átomos que se unen. Hay átomos que se atraen entre sí con mucha fuerza y se unen muy fuertemente y otros que prácticamente no se atraen nada y no se unen.
Enlace metalico
Se produce cuando se unen átomos de un mismo metal, produciéndose estructuras muy compactas formando redes tridimensionales.
Las sustancias metálicas tienen propiedades muy características, como el brillo y la conductividad eléctrica, de aquí se deduce que los electrones implicados en este tipo de enlace deben tener gran libertad de movimiento.
Los átomos de los metales tienen pocos electrones en su última capa, por lo general 1, 2 ó 3. Éstos átomos pierden fácilmente esos electrones y se convierten en iones positivos.
Teoría de bandas:
 Esta teoría representa un modelo más elaborado para explicar la formación del enlace metálico; se basa en la teoría de los orbitales moleculares. Esta teoría mantiene que cuando dos átomos enlazan, los orbitales de la capa de valencia se combinan para formar dos orbitales nuevos que pertenecen a toda la molécula, uno que se denomina enlazante (de menor energía) y otro antienlazante (de mayor energía).
Esta teoría representa un modelo más elaborado para explicar la formación del enlace metálico; se basa en la teoría de los orbitales moleculares. Esta teoría mantiene que cuando dos átomos enlazan, los orbitales de la capa de valencia se combinan para formar dos orbitales nuevos que pertenecen a toda la molécula, uno que se denomina enlazante (de menor energía) y otro antienlazante (de mayor energía).
Enlace covalente
Los enlaces covalentes son las fuerzas que mantienen unidos entre sí los átomos no metálicos (los elementos situados a la derecha en la tabla periódica -C, O, F, Cl, ...).
Estos átomos tienen muchos electrones en su nivel más externo (electrones de valencia) y tienen tendencia a ganar electrones más que a cederlos, para adquirir la estabilidad de la estructura electrónica de gas noble. Por tanto, los átomos no metálicos no pueden cederse electrones entre sí para formar iones de signo opuesto. Un compuesto donde sólo hay enlaces covalentes (y no intermoleculares) está formado únicamente por átomos y se denomina ATÓMICO o COVALENTE. Las fórmulas de estos compuestos son empíricas: representan la proporción de átomos en la red. Por ejemplo la fórmula SiO2 representa que hay doble número de átomos de oxígeno que de átomos de silicio.

Enlace iónico
Este enlace se produce cuando átomos de elementos metálicos (
- Son sólidos con elevados puntos de fusión.
- Son solubles en disolventes polares (agua). Sin embargo, presentan baja solubilidad en disolventes apolares.
- Fundidos y en disolución acuosa conducen la corriente electrica.
- Se obtienen a partir de elementos con distinta electronegatividad (metal y nometal)
miércoles, 5 de febrero de 2014
EL ÁTOMO DE LA ANTIGUEDAD

| 
|
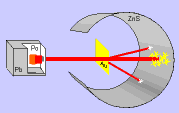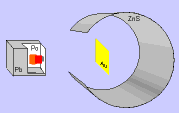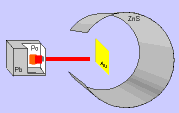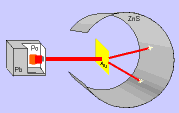
En el siglo V a. C., Leucipo sostenía que había un sólo tipo de materia y pensaba que si dividíamos la materia en partes cada vez más pequeñas, obtendríamos un trozo que no se podría cortar más. Demócrito llamó a estos trozos átomos ("sin división").
La filosofía atomista de Leucipo y Demócrito podía resumirse en:
1.- Los átomos son eternos, indivisibles, homogéneos e invisibles.
2.- Los átomos se diferencian en su forma y tamaño.
3.- Las propiedades de la materia varían según el agrupamiento de los átomos.
|
 |
En el siglo IV a. C., Empédocles postuló que la materia estaba formada por 4 elementos: tierra, aire, agua y fuego.
 | |
 |
Aristóteles, posteriormente, postula que la materia estaba formada por esos 4 elementos pero niega la idea de átomo, hecho que se mantuvo hasta 200 años después en el pensamiento de la humanidad.
 | |
martes, 21 de enero de 2014
EL PETRÓLEO
Como todos sabemos el petróleo se ha formado en muchas épocas atrás se lo comienza a utilizar hace años. La teoría mas aceptada fue por la descomposición de restos de animales y algas microscópicas acumuladas en el fondo de las lagunas y en el curso de los ríos.
El Petróleo es una sustancia oleosa de color muy oscuro compuesta de hidrogeno y carbono y se llama hidrocarburo. Puede hallarse en estado líquido o estado gaseoso, el cual en estado liquido es llamado crudo y se formo como resultado de un complejo químico.
¿Pero en religad que es petróleo? Es un recurso no renovable, como dijimos anteriormente el petróleo es una mezcla de hidrocarburos, compuestos que contienen carbono e hidrogeno. Pero en general el petróleo tal como se extrae de los pozos nos sirve como elegía en la cual es necesario separarlos y de esta manera obtendremos los diferentes combustibles como los que como el gas avión, gasolina, turbosina, diesel, gasoleo ligero y pesado.
Actualmente, el agotamiento de las reservas de pozo de petróleo es un grave problema, pues al ritmo actual de consumo las reservas se agotarían en un promedio de 41 años. Es por eso que los países buscan otra fuente de energía.
lunes, 16 de diciembre de 2013
Suscribirse a:
Comentarios (Atom)